文章出處:公告通知 網(wǎng)責(zé)任編輯: 金飛鷹 閱讀量: 發(fā)表時(shí)間:2025-05-30
近日,四川省經(jīng)濟(jì)和信息化廳、四川省衛(wèi)生健康委員會(huì)等8部門聯(lián)合確定了《四川省創(chuàng)新醫(yī)療器械融合應(yīng)用試點(diǎn)名單(第一批)》并予以公布,包括大腦生理與認(rèn)知功能輔助評估系統(tǒng)、冷凍治療儀、醫(yī)用高分子夾板等器械產(chǎn)品,以下為具體明細(xì):
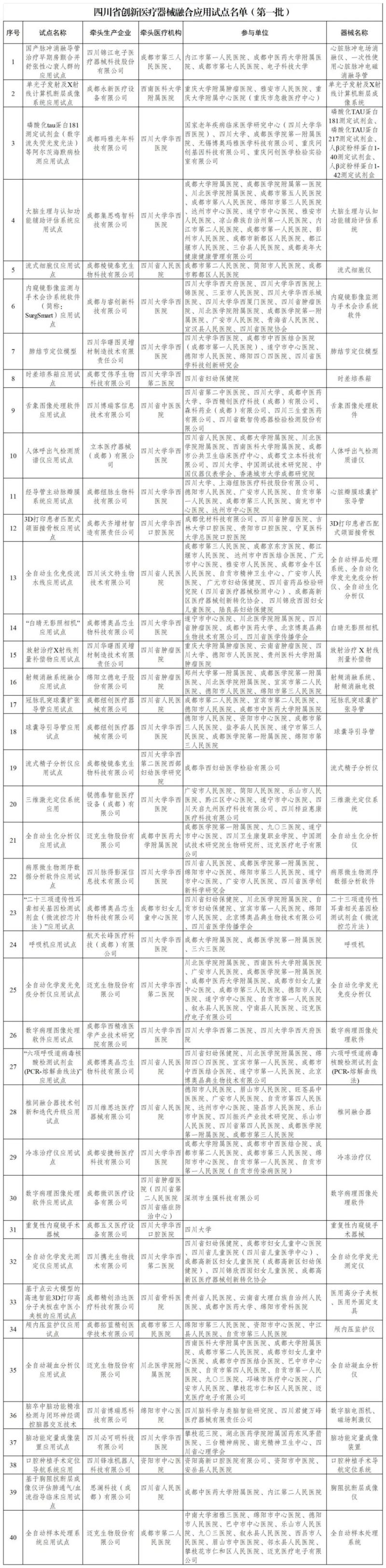
據(jù)悉,這是依據(jù)2024年發(fā)布的《四川省推進(jìn)創(chuàng)新醫(yī)療器械融合應(yīng)用試點(diǎn)實(shí)施方案》(以下簡稱《方案》)開展的創(chuàng)新醫(yī)療器械融合應(yīng)用試點(diǎn)申報(bào)工作。
《方案》申報(bào)方向及實(shí)施內(nèi)容如下:
一、申報(bào)方向
(一)診斷檢驗(yàn)儀器和試劑。
(二)治療裝備和器械。
(三)監(jiān)護(hù)與生命支持裝備。
(四)中醫(yī)診療裝備。
(五)保健康復(fù)裝備。
(六)植介入及口腔醫(yī)療器械。
(七)智慧醫(yī)療、輔助診斷、移動(dòng)醫(yī)療等。
(八)其他類醫(yī)療器械。
二、實(shí)施內(nèi)容
應(yīng)用試點(diǎn)是面向典型應(yīng)用場景,在高端醫(yī)療器械技術(shù)創(chuàng)新與臨床應(yīng)用處于全國前列,對高端醫(yī)療器械醫(yī)工協(xié)同創(chuàng)新、中試驗(yàn)證、臨床應(yīng)用研究、迭代升級與推廣應(yīng)用等具有較強(qiáng)的帶動(dòng)作用,應(yīng)當(dāng)包括但不限于:
(一)數(shù)據(jù)收集對比。對標(biāo)同類先進(jìn)產(chǎn)品的數(shù)據(jù)收集與對比。
(二)建立評價(jià)體系。建立創(chuàng)新醫(yī)療器械在醫(yī)療機(jī)構(gòu)的使用規(guī)范和評價(jià)指標(biāo)體系。
(三)修改完善提升。針對醫(yī)療機(jī)構(gòu)提出的改進(jìn)建議,提升醫(yī)療器械性能水平。
(四)組織人員培訓(xùn)。開展使用人員培訓(xùn),培養(yǎng)應(yīng)用人才。
(五)形成創(chuàng)新成果。形成醫(yī)工融合創(chuàng)新成果,加快創(chuàng)新醫(yī)療器械應(yīng)用。
? 河北藥監(jiān)局抽檢:中頻電療儀等10批次產(chǎn)品不符合標(biāo)準(zhǔn)規(guī)定 ? 未經(jīng)審查發(fā)布醫(yī)療器械&處方藥廣告,廣州一公司被罰42萬! ? 全國首個(gè)醫(yī)療機(jī)構(gòu)應(yīng)用UDI【地方標(biāo)準(zhǔn)】在此落地 ? 體系存在關(guān)鍵缺陷項(xiàng),江蘇兩家醫(yī)械生產(chǎn)企業(yè)被責(zé)令暫停生產(chǎn)! 醫(yī)療器械注冊咨詢認(rèn)準(zhǔn)金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 四川:028 - 68214295 湖南:0731-22881823 湖北:181-3873-5940 江蘇:135-5494-7827 廣西:188-2288-8311 海南:135-3810-3052 重慶:135-0283-7139